 免费试用
免费试用
在当今医疗器械行业,合规性是企业运营的核心要素之一。随着全球对医疗器械安全性和有效性的要求日益严格,各类法规、标准如ISO 13485、FDA 21 CFR 820等相继出台,企业在生产管理过程中面临着前所未有的挑战与机遇。这篇文章将探讨医疗器械生产管理系统如何在满足行业合规标准的同时,提高生产效率和降低运营成本。
痛点共鸣:面临的行业挑战
医疗器械企业在合规管理上常常遭遇以下痛点:
- 复杂的合规要求:不同国家和地区的法规要求不同,企业在产品设计、生产流程、质量管理等方面需不断调整以符合要求。
- 数据追溯困难:传统的手工记录方式使得数据追溯不够及时,难以满足监管机构对生产记录和质量数据的要求。
- 生产效率低下:流程的人工干预和信息孤岛现象导致生产效率低下,增加了不必要的成本。
例如,根据中国信通院发布的《医疗器械行业发展报告》,有超过60%的企业表示合规性管理是其运营中的主要瓶颈 。这不仅影响了企业的市场竞争力,也增加了合规风险。
理论穿透:痛点背后的结构性原因
医疗器械行业的痛点主要源于以下几个结构性原因:
- 法规的快速变化:随着技术的进步,相关法规也不断更新,企业必须随时保持对法规的敏感性与适应能力。
- 技术与管理能力缺乏:许多企业在信息化建设上投入不足,导致生产管理系统无法有效支持合规性需求。
- 信息孤岛现象严重:企业内部各个部门往往独立运作,信息共享不足,导致数据滞后与错误。
例如,超威集团在与轻流合作后,成功实现了生产管理流程的信息化,克服了传统管理模式下的信息孤岛问题,显著提升了合规管理的效率 。
工具验证:无代码平台的解决方案
针对此类问题,轻流无代码平台提供了一种灵活且高效的解决方案。其核心功能特性如下:
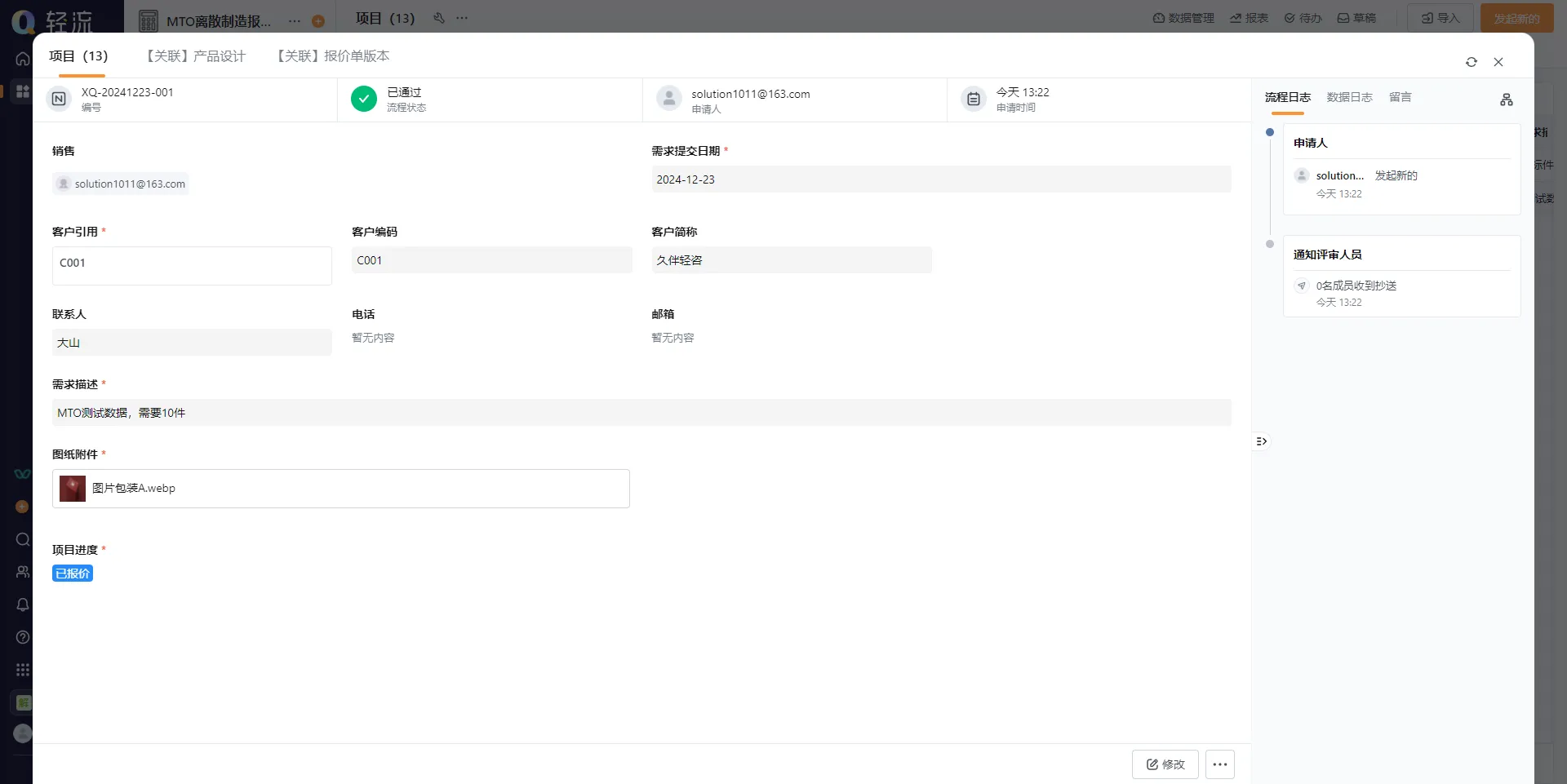
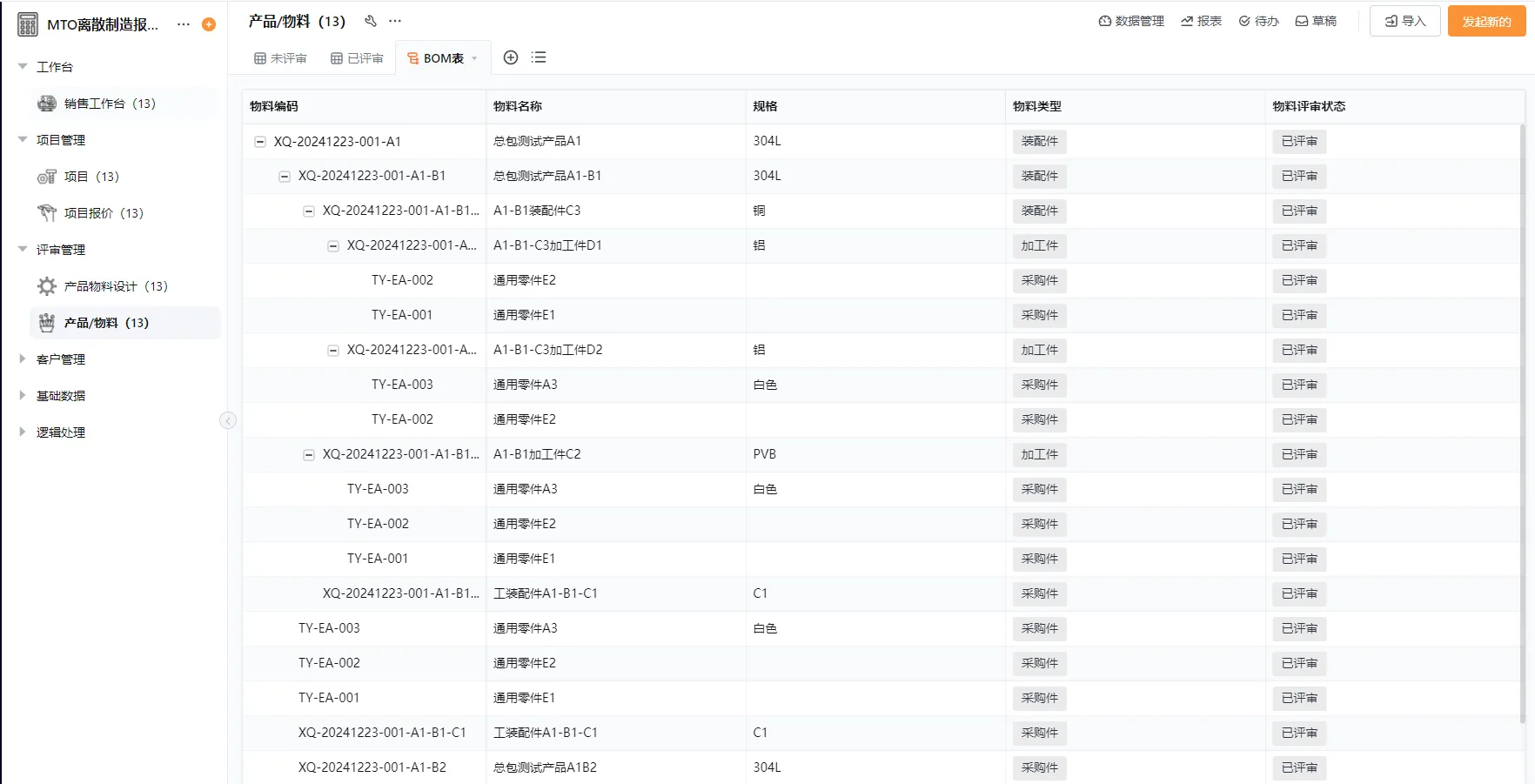
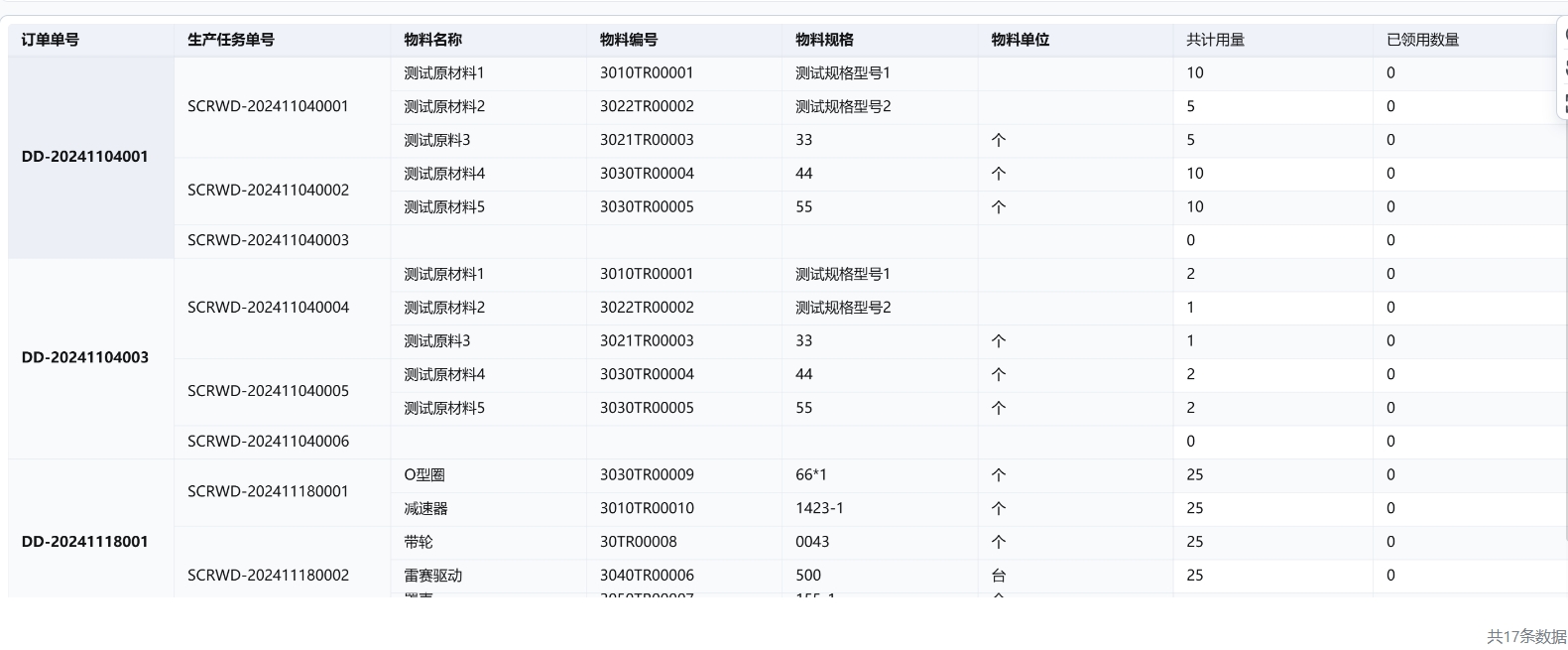
流程自动化:轻流支持自动化的生产流程管理,企业可以根据销售订单自动生成生产工单,确保生产计划的准确性和及时性。这一功能帮助企业降低了人为错误,提升了生产效率。
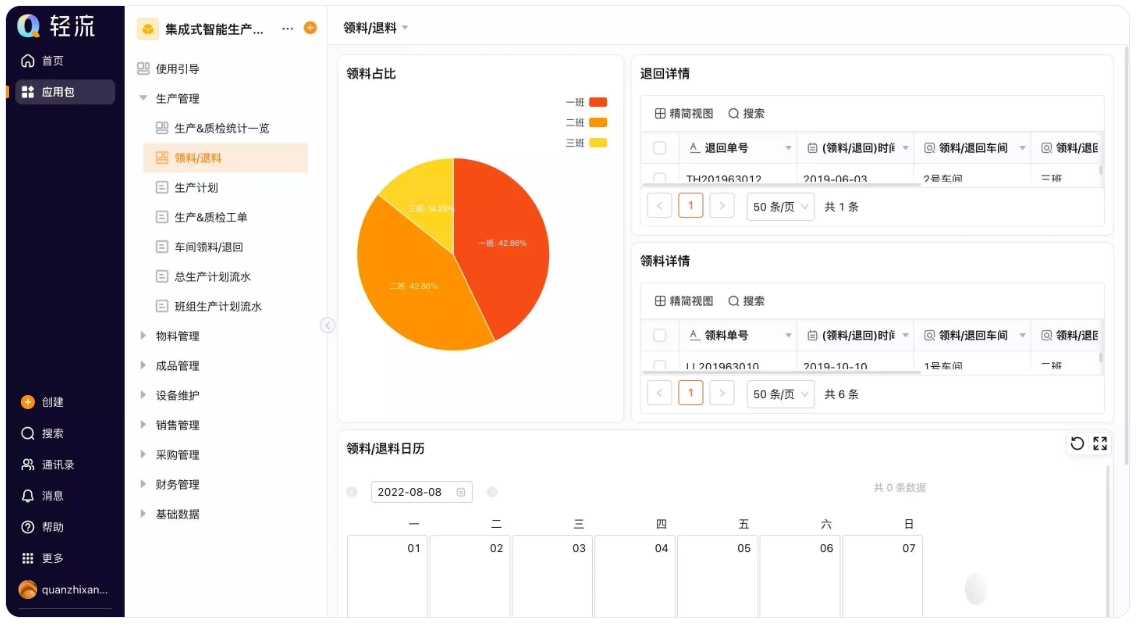
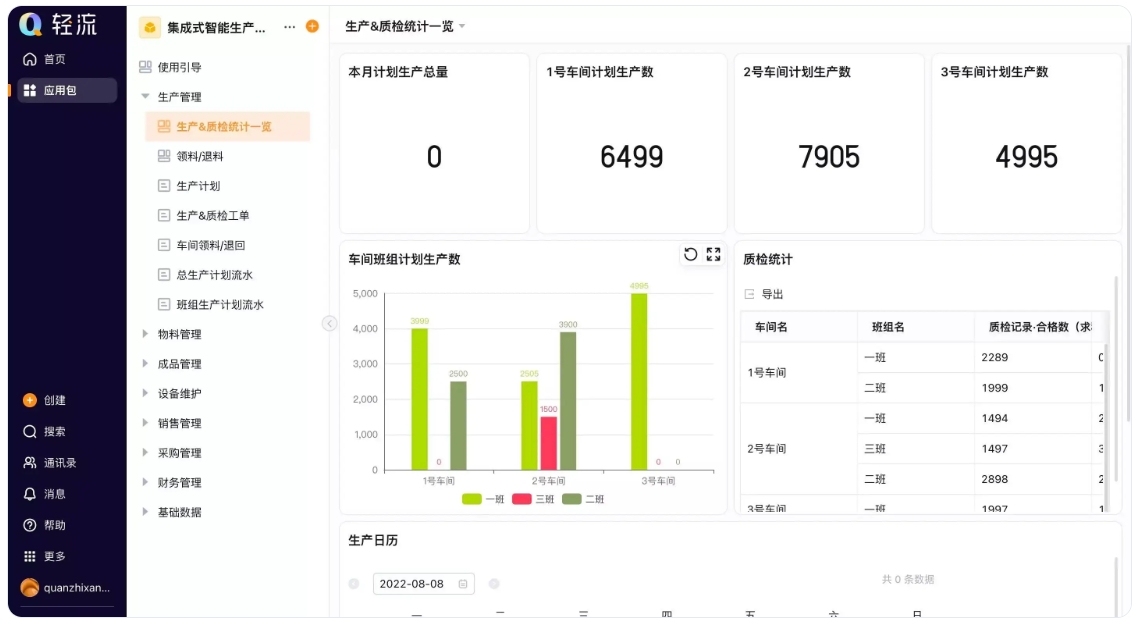
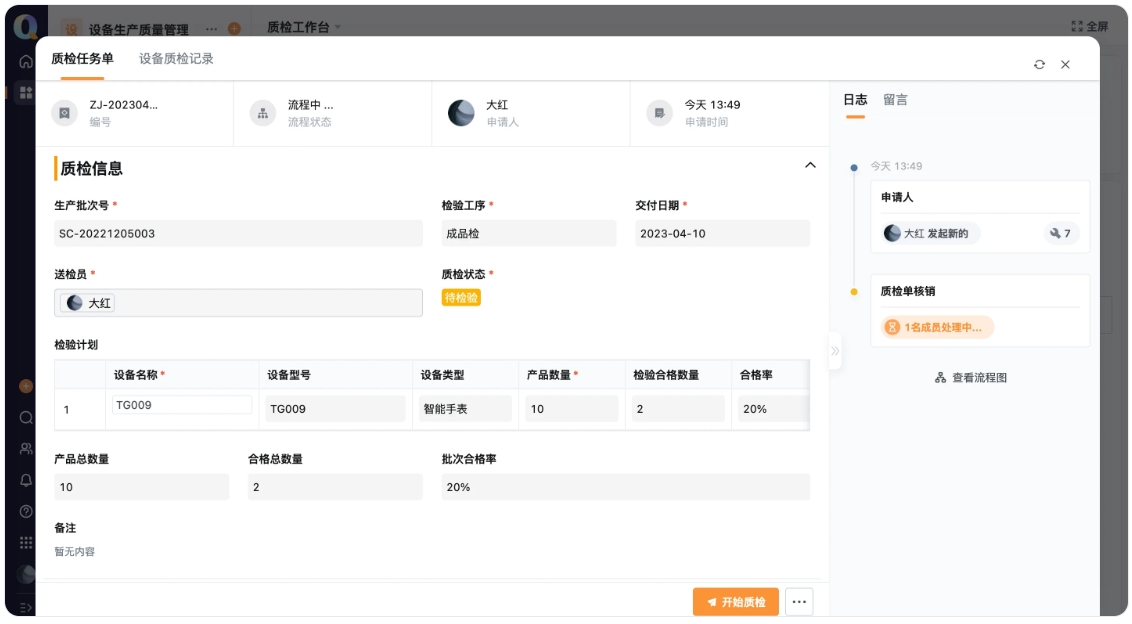
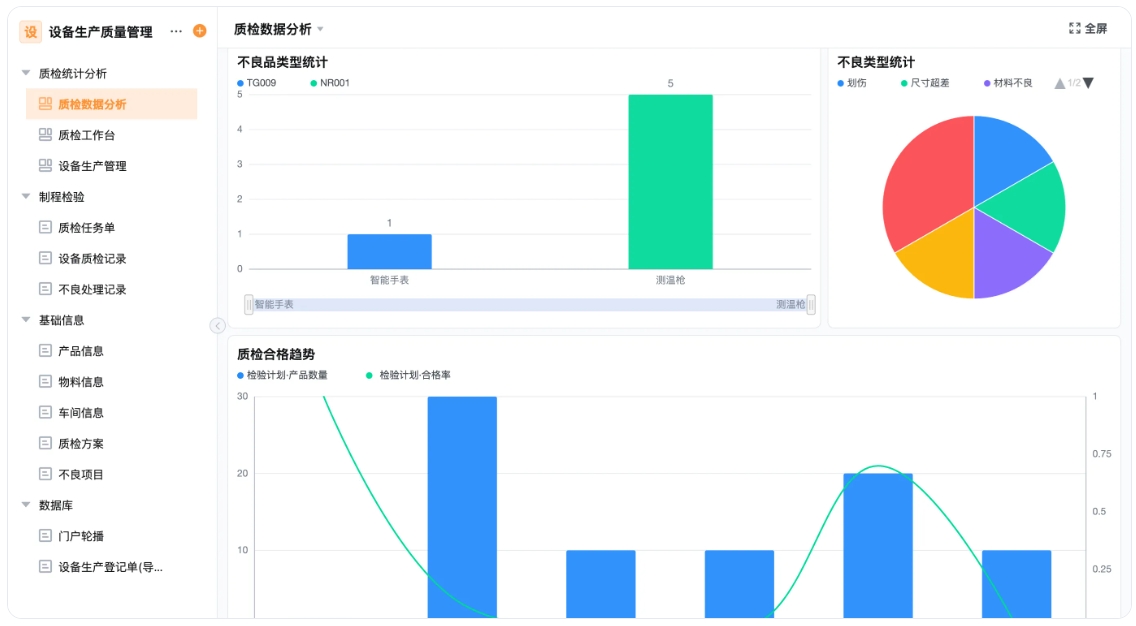
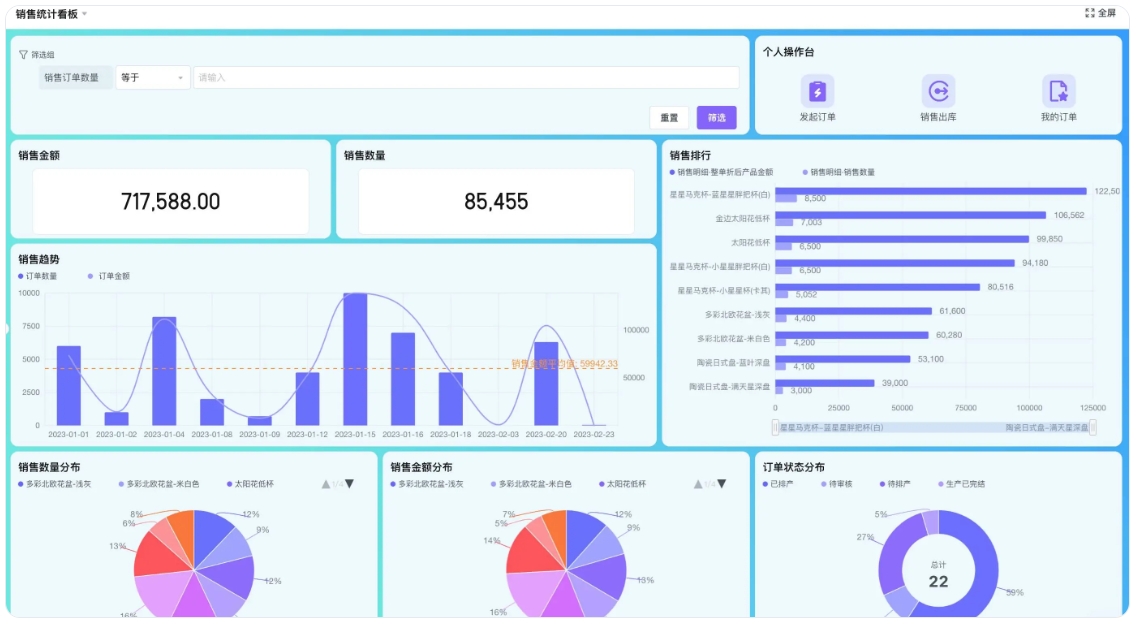
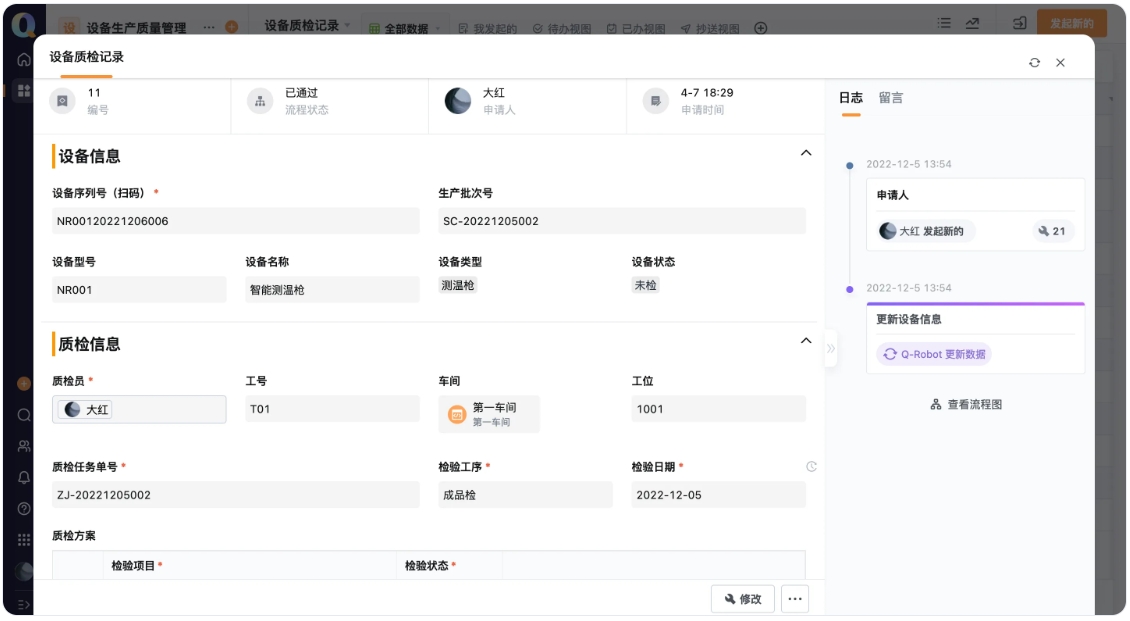
数据可视化:通过可视化的数据看板,管理层可以实时监控生产进度、质量指标及合规性数据,便于快速做出决策。例如,轻流的自定义数据分析看板使得企业能够快速了解设备运行状态、维修记录等,及时发现潜在问题,确保合规性 。
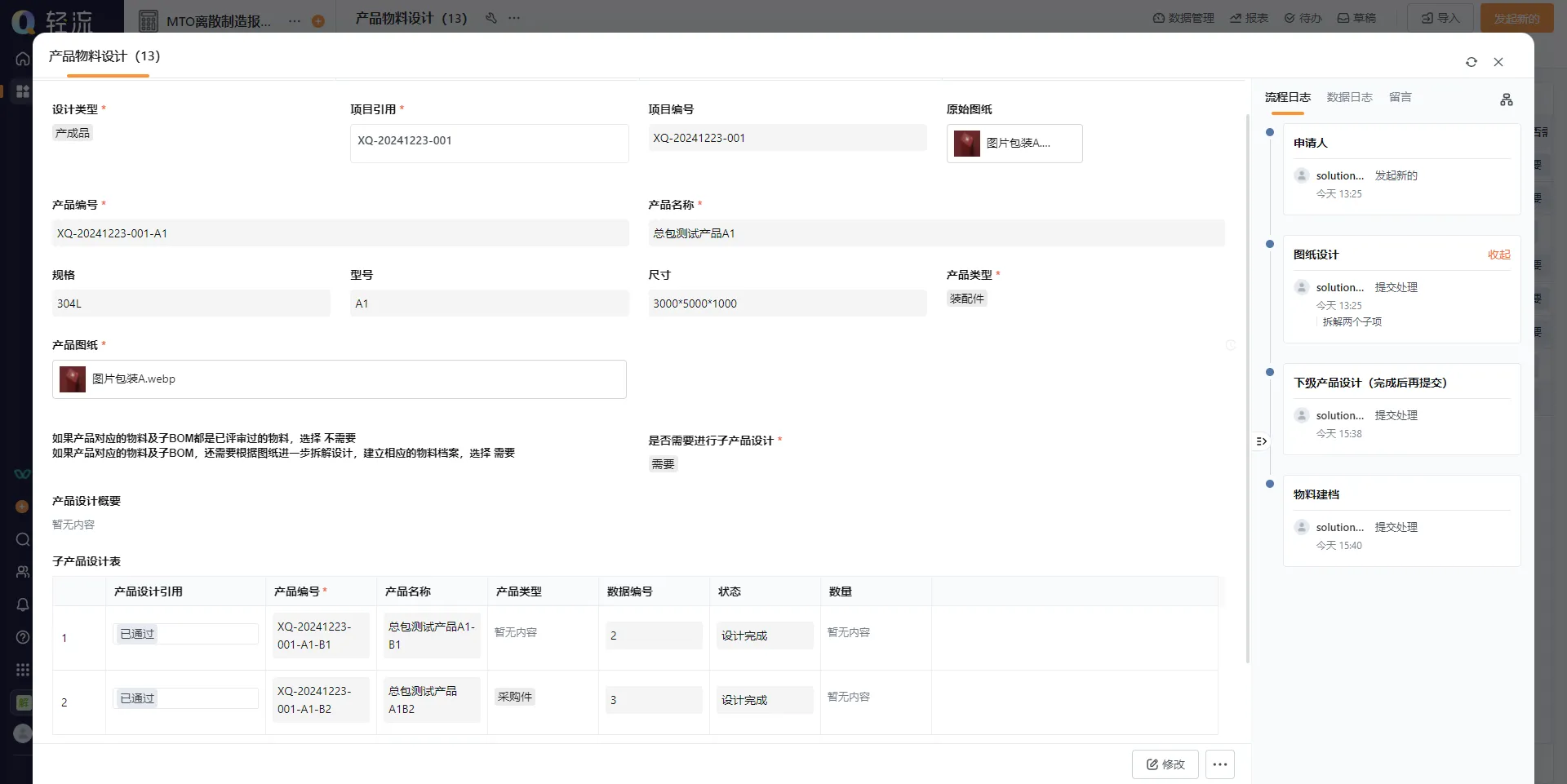
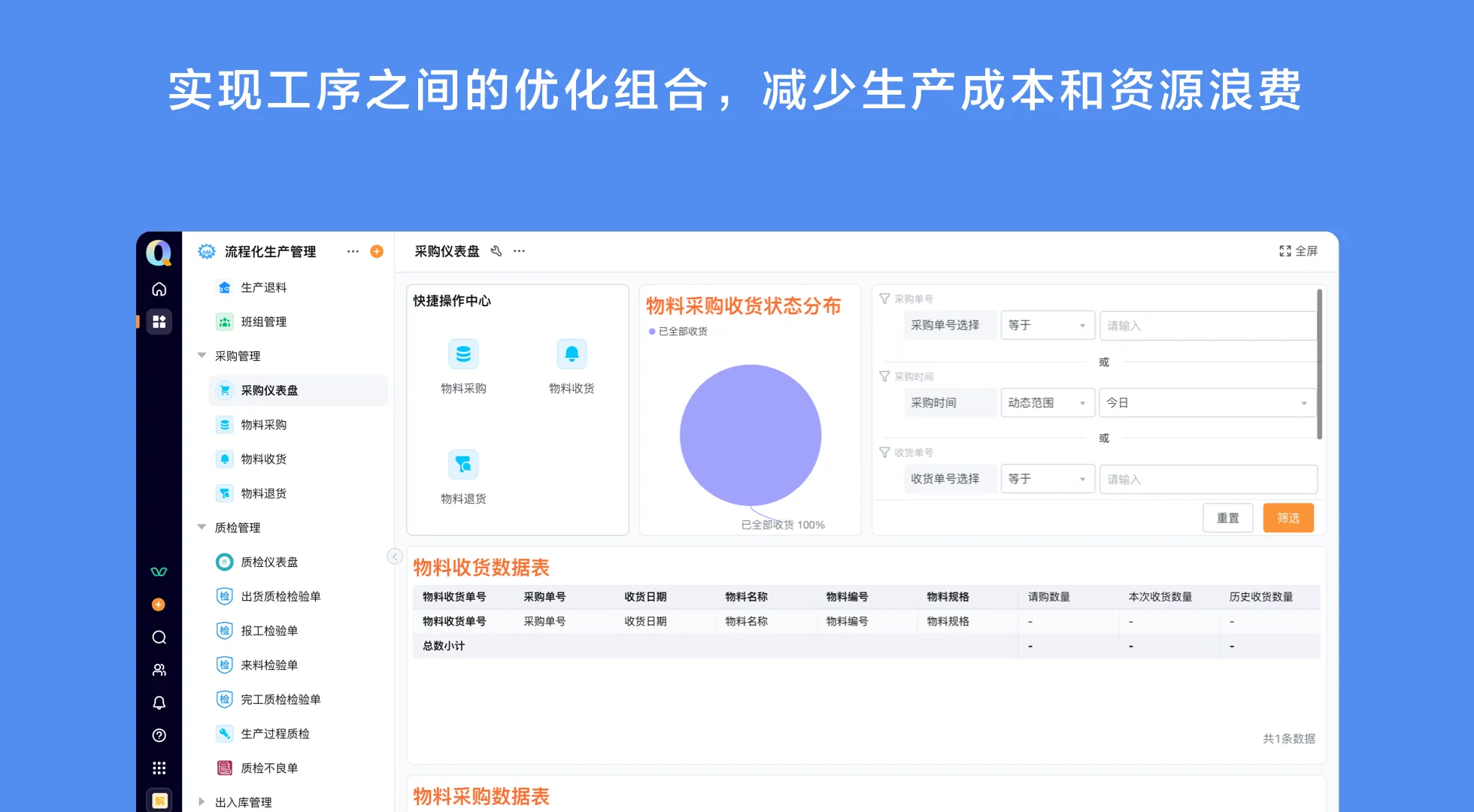
跨系统集成:轻流无代码平台能够与现有的ERP、CRM等系统无缝对接,打破信息孤岛,实现数据的实时共享和自动更新。企业可以在一个平台上管理所有的生产、销售与合规性数据,极大提高了管理效率。
权限管理:平台内置的权限管理功能确保了数据的安全性与合规性,只有授权用户才能访问相关数据,符合监管要求。
展望未来:合规管理的战略导向
未来,医疗器械行业将趋向于更加智能化与数字化的合规管理。政策导向将鼓励企业采用新技术,如人工智能、大数据分析等,来提升合规管理的效率和准确性。根据市场研究机构的报告,到2025年,预计超过50%的医疗器械企业将采用自动化合规管理系统,以应对日益复杂的合规环境。
随着轻流等无代码平台的不断进步,企业将能够更加灵活地应对法规变化,实现合规与效率的双重提升。企业不仅能在合规性上获得保障,还能在市场竞争中占据有利位置。
结语
医疗器械生产管理系统在满足行业合规标准的过程中,不仅仅是提升生产效率的工具,更是企业战略转型的重要组成部分。通过实施无代码解决方案,企业能够灵活应对市场变化,持续提升竞争力。面对未来的挑战,企业需要不断优化管理流程,推动信息化建设,以实现高质量发展。
在这个快速变化的时代,唯有不断进取,才能立于不败之地。


轻客CRM

轻银费控
生产管理

项目管理